标准物质一站式采购平台
- 产品
- 帖子
- 新闻
标准物质一站式采购平台
砷和硒是人体必需的微量元素,摄入量过少或者过多均会影响人体的健康。植物是人体摄取微量元素最重要的途径之一,因此准确测定植物中的砷和硒具有重要意义。
氢化物发生 – 原子荧光光谱法测定砷和硒,具有仪器操作简单、干扰少、普及率高等优点,已广泛应用于环境、地质等领域,成为测定砷和硒的首选方法。
植物样品中砷、硒的消解方法主要有常压湿法消化法和微波消解法等。前者试剂用量大,不利于环境保护;微波消解具有试剂用量少、消解时间短、空白值低、操作简便等优点,已成为植物样品消解的常用方法。当采用氢化物发生 – 原子荧光测定砷和硒时,微波消解后残留的有机颗粒物和硝酸等会对测定造成干扰,因此需要将硝酸赶尽。而消解后的样品加热至蒸干时会造成硒的挥发损失,因此准确控制加热终点是测定植物中砷和硒的关键。
笔者选用微波消解法进行样品处理,减少了试剂用量,降低了样品空白。赶酸时加入高氯酸控制加热终点,当高氯酸冒白烟时停止赶酸,可有效防止硒的挥发损失。消解后的样品加入硫脲,将砷(Ⅴ)还原为砷(Ⅲ)后进行砷的测定。基于此建立了微波消解 – 原子荧光光谱法测定植物样品中砷和硒的含量,方法简便,结果准确、可靠。
1 实验部分
1.1 主要仪器与试剂
原子荧光光谱仪:XGY–1011A 型;
微波消解系统:MARS–Xpress 型;
砷、硒高强度空心阴极灯;
过氧化氢、高氯酸、盐酸和硝酸:优级纯;
砷、硒标准溶液:质量浓度均为 1 000 μg/mL;
砷标准储备液:0.5 μg/mL,将砷标准溶液用20% 盐酸溶液逐级稀释制得;
硒标准储备液:0.1 μg/mL,将硒标准溶液用20% 盐酸溶液逐级稀释制得;
硫脲溶液:称取 80 g 硫脲,溶于 1 000 mL 水中,现用现配;
硼氢化钾溶液:0.7 %,称取 7 g 硼氢化钾,加入2 g 氢氧化钠后溶于 1 000 mL 水中;
实验用水为去离子水,电阻率为 18 MΩ ·cm。
1.2 系列标准工作溶液的配制
系列砷标准工作溶液:分别吸取 0.5 μg/mL砷标准储备液 0.0,0.5,1.0,2.0,4.0 mL 于 100 mL 容量瓶中,加入 20 mL 浓盐酸和 50 mL 硫脲溶液,用去离子水定容,配制成质量浓度分别为 0.0,2.5,5.0,10.0,20.0 ng/mL 的系列砷标准工作溶液。
系列硒标准工作溶液:分别吸取 0.1 μg/mL硒标准储备液 0.0,0.5,1.0,2.0,4.0,8.0 mL 于 100mL 容量瓶中,加入 20 mL 浓盐酸,用去离子水定容,配制成质量浓度分别为 0.0,0.5,1.0,2.0,4.0,8.0ng/mL 系列硒标准工作溶液。
1.3 仪器工作条件
氢化物发生原子荧光光谱仪测定砷和硒的工作条件见表 1。
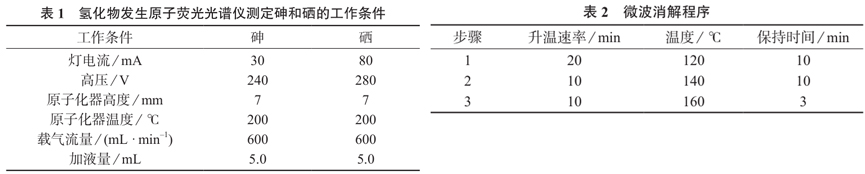
1.4 分析步骤
称取 0.250 0 g 植物样品于 10 mL 微波消解罐中,依次加入 2 mL 硝酸和 0.5 mL 过氧化氢,于室温放置 1 h 进行预消解,然后按表 2 微波消解程序进行消解。消解完毕后,冷却至室温,在通风橱内缓慢旋开密封盖,将溶液转移至 25 mL 锥形瓶中,再加入 1 mL 高氯酸,置于 240℃电热板上加热至高氯酸冒白烟为止。取下冷却片刻后加入 2 mL 盐酸溶液(1∶1),再置于电热板上加热至溶解,取下冷却至室温,用去离子水定容于 10 mL 比色管中,摇匀后静置。
分取 5 mL 试液于 10 mL 比色管中,加入 2 mL硫脲溶液,放置 2 h,充分还原后测定砷。
另取剩余试液 2 mL 直接测定硒。
2 结果与讨论
2.1 消解体系选择
硫酸沸点较高,在密闭的消解罐中易产生高温损坏消解罐;高氯酸在高温下分解并产生较大压力,密闭消解时易发生爆炸;盐酸难以消解植物样品中的有机物。因此以上 3 种酸均不适用于微波消解植物样品。
硝酸是植物样品消解最常用的强氧化酸,在硝酸中加入过氧化氢可以大幅度提高其氧化能力,使在纯硝酸体系中不能消解完全的样品得到充分消解。因此本实验选用硝酸 – 过氧化氢混合液(4∶1)进行消解。
2.2 仪器工作条件选择
2.2.1 原子化器预加热温度
原子化器预加热温度会影响测定的灵敏度,不同的原子化器预加热温度对应的荧光强度如图 1。
由图1可知,在 50~200℃范围内,砷和硒的荧光强度随温度增大而不断增加,随原子化预加热温度的增加氢化物传输效率不断提高,因此分析灵敏度不断增加。200℃以后随温度增大荧光强度不断下降,可能是因为生成的氢化物受热分解,火焰中总的基态原子数减少,所以被检测到的荧光信号变弱。当温度高于 300 ℃时记忆效应变大。因此实验选择原子化器预加热温度为 200℃。
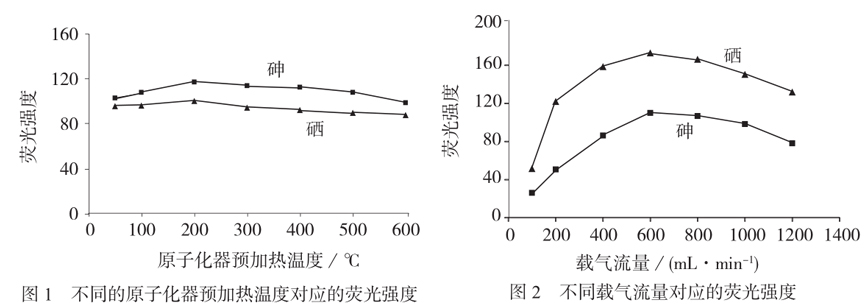
2.2.2 载气流量
固定其它条件不变,只改变载气流量,荧光强度随载气流量的变化结果如图 2 所示。由图 2 可知,当载气流量小于 600 mL/min 时,随着载气流量的增大,氢化物传输效率不断提高,荧光强度不断增加;当载气流量为 600 mL/min 时荧光强度最大;当载气流量大于 600 mL/min 时,荧光强度逐渐降低,可能是流量过大的载气稀释氢化物所致。因此载气流量选择为 600 mL/min。
2.3 线性方程与检出限
在 1.3 仪器工作条件下,分别测定系列砷、硒标准工作溶液,以溶液的质量浓度为自变量(x,ng/mL)、荧光强度为因变量(y)进行线性回归,计算线性方程和线性相关系数。按照样品分析程序,平行制备 12 份空白样品并测定砷和硒,计算测定值的标准偏差,以 3 倍标准偏差计算方法检出限(稀释因子 40 倍)。砷、硒的线性范围、线性方程、相关系数、检出限列于表 3。
2.4 精密度试验
选取国家一级标准物质 GBW 10016(茶叶),平行称取 12 份,按照 1.4 分析步骤,测定砷和硒的含量,测定结果见表 4。由表 4 可知,砷、硒测定结果的相对标准偏差分别为 3.65%,3.52 %,表明本法精密度良好。
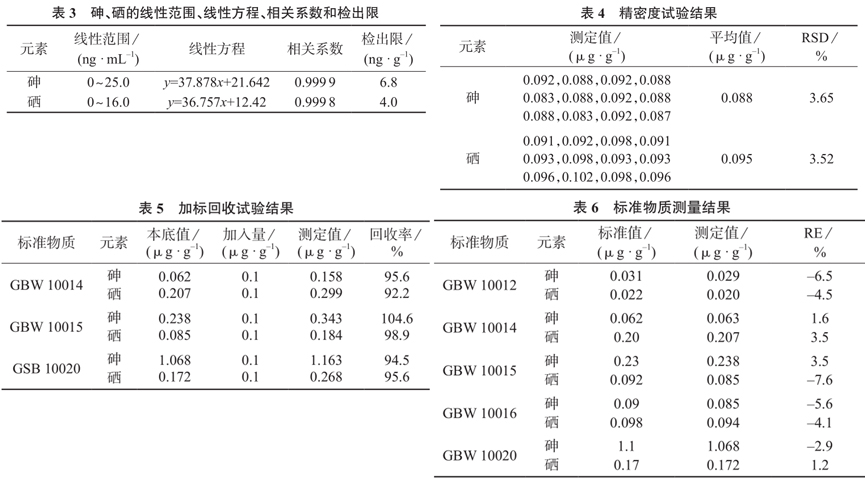
2.5 加标回收试验
对国家一级标准物质 GBW 10014 (圆白菜)、GBW 10015(菠菜)、GBW 10020 (柑橘叶)进行砷和硒的加标回收试验,结果列于表 5。由表 5 数据可知,砷、硒的加标回收率分别为 94.5%~104.6%,92.2%~98.9%,表明本法测定结果准确度较高。
2.6 对照试验
选取 5 种国家一级标准物质样品玉米(GBW10012)、圆白菜(GBW 10014)、菠菜(GBW 10015),茶叶(GBW 10016)、柑橘叶 (G BW 10020),按照 1.4步骤处理,在 1.3 仪器工作条件下测定其中砷、硒的含量,测定结果列于表 6。由表 6 可知,砷、硒测定值与标准值基本一致,表明本方法准确、可靠。
3 结语
选用微波消解作为植物样品的前处理方法,减少了试剂用量,降低了样品空白,赶酸过程加入高氯酸,加热至高氯酸冒白烟,可有效防止硒的挥发损失。所建立的微波消解 – 原子荧光光谱法测定植物样品中的砷和硒,经国家一级标准物质验证,该方法灵敏度高,测定结果准确、可靠。

2024年7月16-18日,在河南省周口市举办的”第九届全国大学生生命科学竞赛(2024,科学探究类)河南省赛区决赛”圆满落幕!BNCC邀您重温精彩瞬间!
了解更多> >通话对您免费,请放心接听
温馨提示:
1.手机直接输入,座机前请加区号 如13164239859,010-58103778
2.我们将根据您提供的电话号码,立即回电,请注意接听
3.因为您是被叫方,通话对您免费,请放心接听

登录后才可以评论