标准物质一站式采购平台
- 产品
- 帖子
- 新闻
标准物质一站式采购平台
萤石是一种钙的天然卤素化合物,是工业上用途广泛的氟化物。在新能源、国防、新材料、制冷、电子、光学、医药、通讯、建材、陶瓷等工业领域均有着重要的作用,其检测手段一直受到各行业研究人员的重视。
目前萤石中氟化钙的检测一般采用 X 射线荧光法、ICP–AES 法、离子色谱法、EDTA 滴定法等。由于萤石矿石中通常存在部分含钙碳酸盐矿物和含钙硅酸盐矿物,故对萤石矿石中氟化钙的分析普遍采用 EDTA 滴定法 (GB/T 5195.1–2006 《萤石氟化钙含量的测定》),该方法溶解样品的过程:先用稀乙酸浸取分离掉碳酸钙,然后用AlCl3浸取萤石或以硼酸–盐酸浸取,将测定浸取液中的钙换算成 CaF2。在实际操作中,此溶解方法存在一些问题:用于分离氟化钙和碳酸钙的乙酸溶液,也能溶解部分氟化钙,而且对于氟化钙的溶解量因碳酸钙的含量不同而异,现有的方法一般采用经验补正0.3%,对于不同基质样品会有较大误差;对于碳酸钙含量高的样品使用乙酸溶液浸取,达不到完全浸取的效果,溶解不完全,导致分析结果误差较大。采用 X 射线荧光法、ICP–AES 法测定氟化钙往往没有考虑萤石中其它钙盐的含量或者使用校正系数的手段,故在以钙总含量计氟化钙含量的方法中,此溶样手段均会导致检测结果的不准确,因此需要建立一种适用范围广泛的氟化钙分析方法。笔者采用稀盐酸溶解样品,通过调节 pH 以及加入氯化钙溶液沉淀氟化钙,用 EDTA 法滴定,建立了一种准确测定高含量碳酸钙基体中氟化钙的方法。该法直接溶解碳酸钙,改变了物相层层剥离方式,避免了碳酸钙基体干扰氟化钙测定的问题。
1 实验部分
1.1 主要仪器与试剂
氟离子选择性电极:PXS–270 型;
气体收集器:25 mL;
分析天平:BS124S 型,感量为 0.0001 g;
恒温电热板:CT1461–35 型;
控温水浴锅:DZKW–4 型厂;
盐酸、氢氧化钠、氢氧化钾、氯化钙、三氯化铝、蔗糖,三乙醇胺:分析纯;
EDTA 标准溶液:c(C10H14N2O8Na2 ·2H2O)=0.015 mol/L,称取 5.58 g 乙二胺四乙酸二钠盐于 400 mL烧杯中,加适量水溶解,移入 1 000 mL 容量瓶中,用水稀释至标线,混匀;
钙黄绿素–百里酚酞指示剂:称取 0.25 g 钙黄绿素、0.12 g 百里酚酞、20 g 硫酸钾置于玛瑙研钵中研磨混匀,贮于磨口瓶中,保持干燥;
萤石准物质:编号为 GBW 07251,CaF2 含量90.87%;
白云石标准物质:编号为 GBW 07216a(CaCO3含量以 CaO 记 ),CaO 含量为 35.02%;
实验所用试剂除注明外均为分析纯;
实验用水为去离子水。
1.2 标准样品及制备
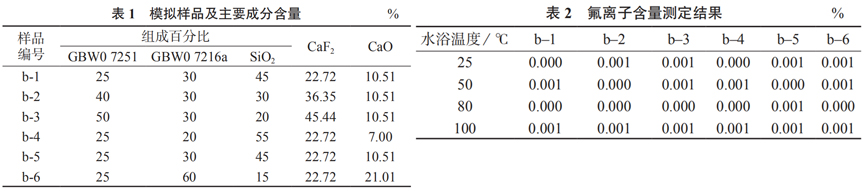
用萤石标准物质和白云石标准物质按一定比例配制 6 组高含量碳酸钙基体含氟化钙的模拟样品,辅料为光谱纯的 SiO2,粒度均在 75 μm(200 目 )以下,氟化钙含量控制在 10%~60% 之间,编号分别为 b–1,b–2,b–3,b–4,b–5,b–6,见表 1。
1.3 实验方法
准确称取 0.3000 g 样品于 100 mL 烧杯中,加入 10 mL HCl 溶液 (1+9),盖上表面皿,在沸水浴上加热 30 min,每隔 5 min 用玻璃棒搅拌一次,取下,用少量水洗涤表面皿后。用 NaOH (4.0 g/L) 中和至合适的酸度,用酸度计准确测定。加入适量CaCl2 溶液 (0.10 mol/L),使 CaF2 沉淀完全,静置过夜,过滤,用水洗涤 5~6 遍,将沉淀连同滤纸一同转
入原烧杯。加入20 mL中性三氯化铝溶液(80 g/L),盖上表面皿,置于电热板上煮沸,转至水浴锅中沸水浴,时常搅拌,并加水控制体积不变。1 h 后取下,冷却至室温,过滤,用 250 mL 容量瓶承接滤液,定容,摇匀。移取 100 mL 溶液至 250 mL 烧杯中,依次加入 15 mL 蔗糖溶液 (150 g/L),10 mL 三乙醇胺溶液 (1+2),20 mL KOH 溶液 (200 g/L),加少许钙黄绿素–百里酚酞指示剂,在黑色背景下,用 0.02000 mol/L EDTA 标准溶液滴至荧光绿色消失,溶液变为紫红色为终点。
2 结果与讨论
2.1 加热温度对氟离子的影响
当采用稀盐酸溶解样品时,样品中被溶解的碳酸钙会产生气体,若氟离子与其它气体一起挥发,则方法不可行。因此有必要检验溶解样品气体中是否存在氟离子。称取模拟样品 0.3000 g 于 50 mL 比色管中,加入 10 mL HCl 溶液 (1+9),每个比色管上加一套放有氢氧化钠的气体收集装置用于收集稀盐酸溶样时产生的气体,分别在 25,50,80℃沸水浴中加热 30
min,调节收集器中溶液的酸度,用氟离子选择性电极进行测定,结果列于表2。由表2可知,不同水浴温度下氟离子基本没有损失。
2.2 pH 值对氟化钙沉淀的影响
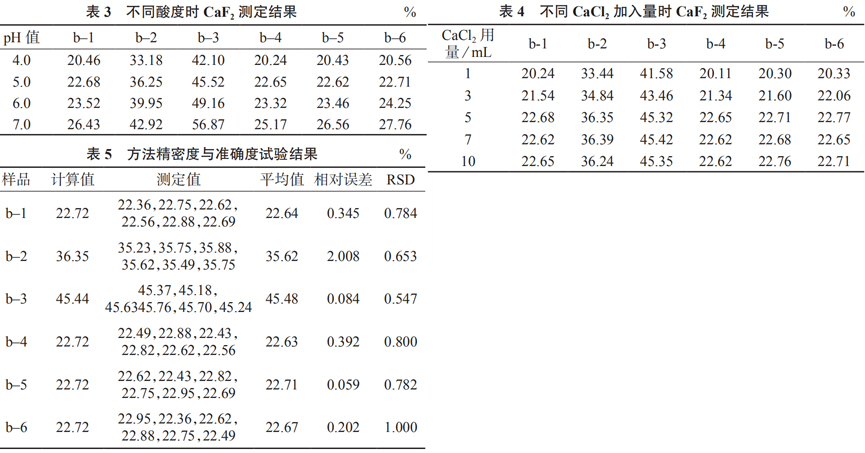
将水浴后的样品,用 NaOH 溶液 (4.0 g/L) 中和,分别调节 pH 值为 4.0,5.0,6.0,7.0 的不同酸度,按照1.3 实验方法进行测定,结果见表 3。对照表 1、表 3数据可知,当 pH 值为 5.0 时,测定结果最理想。这可能是因为当 pH 值小于 5 时,溶液中存在多余的氢离子,会使氟化钙沉淀困难;而随着 pH 值的增大,氟化钙沉淀逐渐增大,但当 pH 值大于 5 时,过多的氢氧根离子也会导致大量的钙离子沉淀,导致结果偏高。
2.3 氯化钙加入量对氟化钙测定的影响
将 0.300 0 g 样品用 (1+9) 盐酸溶液溶解,用氢氧化钠溶液 (4.0 g/L) 中和至 pH5.0,向样品中加入不同量氯化钙(0.10 mol/L) 溶液,用量分别为 1,3, 5,7,10 mL,分别测定,结果见表 4。由表 4 可知,氯化钙加入量大于 5 mL 时检测结果准确。可能因为酸过量时,氟化钙部分溶解,而当 pH 值调节至 5.0时,使溶解的氟化钙重新生成沉淀。此时碳酸钙中碳酸根反应完全,而钙以氯化物形式存在于溶液中,加入一定量氯化钙,可增加钙离子浓度,使化学反应向生成氟化钙方向移动,使氟化钙沉淀完全。综合考虑,选择氯化钙的加入量为 5 mL。
2.4 方法精密度与准确度试验
称取 0.300 0 g 样品,按 1.3 实验方法进行 6 次平行测定,测定结果及相对标准偏差见表 5。由表 5 可见,测定结果均与计算值相符,相对误差为0.059%~2.008%,测定结果的相对标准偏差不大于1%,符合方法设计要求。
3 结语
利用稀盐酸溶液直接溶解样品中碳酸钙,调节酸度,利用氯化钙辅助沉淀氟化钙,建立了高含量碳酸钙基体中氟化钙的测定方法。该方法测定结果不受基体干扰,检测快速,准确度、精密度较高,适用于基体碳酸钙含量较高时氟化钙的测定。

由天津国际生物医药联合研究院主办,商城北纳创联生物科技有限公司承办的“(京津冀)生物制造产业发展论坛”,定于2024年7月24日在天津国际生物医药联合研究院召开。
了解更多> >为加快公司高级技能人才培养,提高专业技能素质,充分调动员工的工作热情和积极性,推动公司科技进步和技术创新,北纳生物专业技术等级评定于2019年12月7日下午两点正式举行。
了解更多> >为了适应企业发展的需要以及更好的满足客户需求,北纳生物经过不断地开发与完善,分别对BNCC官网www.bncc.org.cn及北纳标物网www.biaowu.com进行了新的升级改版,极大地方便了新老客户朋友们的操作及使用。
了解更多> >通话对您免费,请放心接听
温馨提示:
1.手机直接输入,座机前请加区号 如13164239859,010-58103778
2.我们将根据您提供的电话号码,立即回电,请注意接听
3.因为您是被叫方,通话对您免费,请放心接听

登录后才可以评论